o Que é Rutênio
Um metal de transição, rutênio (pronuncia-roo-A-nee-em) é denotada pelo símbolo químico Ru . Estima-se que a sua abundância na crosta terrestre seja de 1×10-7 % . É um dos metais preciosos, pertencente à família da platina que também inclui ródio, paládio, ósmio e irídio . A EF é frequentemente utilizada na forma de folhas, folhas e varetas para sua alta ductilidade.,

Rutênio Símbolo
É um Elemento Radioativo

Rutênio Metal
, Onde é Rutênio Encontrados na Natureza
Ele pode ser encontrado perto da platina depósitos nos Montes Urais da Rússia, e na américa do Norte e América do Sul. Ele também é extraído como um subproduto da mineração de níquel em Sudbury Basin, Ontário, Canadá .,
História do Rutênio
de Origem
o Seu nome foi derivado do nome latino para a Rússia, Rutênia .
Who discovered it
While investigating a sample of platinum ore residue from South America, the Polish chemist Jedrzej Sniadecki discovered a new element vestium in May 1808. No entanto, ele retirou sua alegação de descoberta quando a mesma pesquisa sobre o minério feito por alguns químicos franceses não produziu nenhum resultado.,
mais Tarde, em 1825, Gottfried Osann da Universidade de Dorpat (agora Tartu), examinou algumas platina depósitos de minério de Montanhas Ural e encontrou três novos elementos que foram denominados de pluranium, polinium, e rutênio, respectivamente. Karl Karlovich Klaus, em 1840, na Universidade de Kazan, confirmou que a EF era um metal original após sua extração e purificação, mantendo o mesmo nome, enquanto os outros dois elementos nunca foram verificados .,7f3f8e3″>Period

Location of Ruthenium in the Periodic Table
Properties and Characteristics of Ruthenium
General Properties |
|||||||||||||||
| Relative Atomic Mass (Atomic Weight) | 101.,07 | ||||||||||||||
| Molar Weight (g/mol) | 101.,d> | Metallic | |||||||||||||
| Odor | Unknown | ||||||||||||||
| Malleability | Yes | ||||||||||||||
| Ductility | Yes | ||||||||||||||
| Melting Point (°C) | 2333 | ||||||||||||||
| Boiling Point (°C) | 4147 | ||||||||||||||
| Density (g/cm3) | 12.,1 | ||||||||||||||
| State of Matter at Room Temperature (Solid, Liquid, or Gas) | Solid | ||||||||||||||
| Young’s Modulus (GPa) | 447 | ||||||||||||||
| Hardness (Mohs) | 6. 5 | ||||||||||||||
| Electrical Conductivity (Sm-1) | 14.9 × 10-6 | ||||||||||||||
| Resistivity (Ω m) | 15., | – m ℓ | -1 | ||||||||||||
| – m s | -1/2 | ||||||||||||||
| Electron Configuration | 4d75s1 | ||||||||||||||
| Primary XPS Region | Ru3d | ||||||||||||||
| Crystal Structure | hcp: hexagonal close packed | ||||||||||||||
| Lattice Constants (Parameters) (pm) | 270.,59, 270.59, 428.,Fifth Energy Level | 1 | |||||||||||||
| Ionic Charge | |||||||||||||||
| – Ruthenium (III) | +3 | ||||||||||||||
| – Ruthenium (IV) | +4 | ||||||||||||||
| Radius of Atom | |||||||||||||||
| – Atomic Radius (Å) | 2.,13 | ||||||||||||||
| – Covalent Radius (Å) | 1.36 | ||||||||||||||
| Electron Affinity | 101.31 | ||||||||||||||
| Electronegativity | 2.,2 | ||||||||||||||
| Ionization Energy | 1st | 2nd | 3rd | 4th | 5th | 6th | 7th | ||||||||
| 710.18 | 1617.09 | 2746.,94 | – | – | – | – | |||||||||
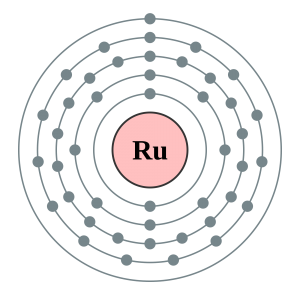
Ruthenium Bohr Model
What is Ruthenium Used for
Uses of the Element and its Compounds
As an alloying agent – Addition of 0.,1% da EF aumenta a resistência à corrosão do titânio em cem vezes, enquanto o seu uso no fortalecimento da platina e paládio ajuda na fabricação de contatos elétricos resistentes ao desgaste, bem como para revestimento de jóias e acabamento . Uma liga de rutênio, ouro e paládio também é aplicável para fazer rebites e tiras com cabeça de estalar.
Jóias de ruténio
como catalisador – tem um uso catalítico na produção de ácido acético e amônia. O metal também tem um uso laboratorial como um catalisador em sua forma de dióxido .,
para a produção de cloro – ânodos revestidos por óxido de ruténio em células electroquímicas são utilizados para a produção em grande escala de cloro .as ligas à base de implantes dentários podem ser úteis como materiais de implante para cirurgias dentárias. No entanto, é necessário um teste do sistema transdérmico para determinar a alergia de contacto antes da utilização .
na forma de corantes complexos-a utilização de corantes à base de compostos de ruténio em células solares sensibilizadas por corantes promove a conversão da luz solar em electricidade a um custo inferior .,
electrodeposited rutenium black em prata revestida a ouro pode ser eficaz como um eletrodo substituto da platina para a produção industrial de hidrogênio através da eletrólise da água, devido às suas propriedades eletrocatalíticas. No entanto, existem algumas questões de viabilidade relativamente à sua utilização comercial .

Jóias de ruténio Negro
vermelho de ruténio é utilizado para coloração de matérias animais e vegetais . Alguns outros compostos da EF também são usados para colorir vidro e cerâmica .,
pelas suas propriedades anti-cancro-dois medicamentos à base de ruténio, NAMI-a e KP1019, que exibem actividade anti-cancro, foram produzidos em laboratório, mas ainda se encontram na fase de ensaios clínicos em seres humanos . Rutênio porfirina, quando usado como um fotossensibilizador, pode ajudar na destruição de células cancerosas .
em baterias recarregáveis – nitreto de rutênio tem o potencial de desempenhar o papel de um eletrodo para baterias de Íon lítio, bem como supercapacitores .,
é tóxico por ruténio
ruténio (incluindo um dos seus radioisótopos Ru-106) e os seus compostos podem ter propriedades carcinogénicas que podem causar riscos a longo prazo para a saúde e também sofrer reacções violentas com outros produtos químicos. A ingestão do metal pode levar à sua acumulação gradual nos ossos, pelo que deve ser manuseada com cuidado, uma vez que os seus fumos podem causar irritação na boca, pulmões, pele e olhos.,

Rutênio Anel
curiosidades
- Rutênio boride (RuB) filmes têm uma dureza de 50 Gpa, que é maior do que a massa Rutênio constituídos por boretos, um grupo de compostos de boro conhecido por sua dureza .em uma pesquisa, uma solução de tricloreto de rutênio e derivados de benzimidazol foi encontrada para produzir novos compostos de EF que atuam como paramagnetos .,

Ruthenium Pictures
Ruthenium Price
The element costs between $120 and $130 per 100g in its purest form.