La solubilità dei soluti dipende dalla temperatura. Quando un solido si dissolve in un liquido, avviene un cambiamento nello stato fisico del solido analogo alla fusione. Il calore è necessario per rompere i legami che tengono insieme le molecole nel solido. Allo stesso tempo, il calore viene emesso durante la formazione di nuovi legami soluto-solvente.,
- CASO I: Diminuzione della solubilità con la temperatura: Se il calore emesso nel processo di dissoluzione è maggiore del calore necessario per rompere il solido, la reazione netta di dissoluzione è esotermica (energia emessa). L’aggiunta di più calore (aumenta la temperatura) inibisce la reazione di dissoluzione poiché il calore in eccesso viene già prodotto dalla reazione. Questa situazione non è molto comune dove un aumento della temperatura produce una diminuzione della solubilità.,
- CASO II: Aumento della solubilità con la temperatura: Se il calore emesso nella reazione di dissoluzione è inferiore al calore necessario per rompere il solido, la reazione di dissoluzione netta è endotermica (energia richiesta). L’aggiunta di più calore facilita la reazione di dissoluzione fornendo energia per rompere i legami nel solido. Questa è la situazione più comune in cui un aumento della temperatura produce un aumento della solubilità per i solidi.
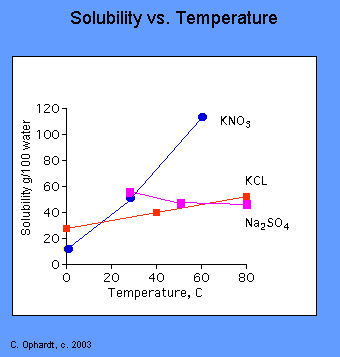
Figura: solubilità dipendenti dalla temperatura di tre sali in acqua.,
L’uso di impacchi freddi istantanei di pronto soccorso è un’applicazione di questo principio di solubilità. Un sale come il nitrato di ammonio viene sciolto in acqua dopo un forte colpo rompe i contenitori per ciascuno.
\
La reazione di dissoluzione è endotermica e richiede calore. Pertanto il calore viene prelevato dall’ambiente circostante e il pacchetto si sente freddo.
Contributori e attribuzioni
Charles Ophardt (Professore emerito, Elmhurst College); Chembook virtuale