Caut Apropiat: Apă, cel Mai Important Lichid
Pământul este singurul corp din sistemul nostru solar care are apă lichidă existente în mod liber pe suprafața sa. Acesta este un lucru bun, deoarece viața pe Pământ nu ar fi posibilă fără prezența apei lichide.apa are mai multe proprietăți care o fac o substanță unică printre substanțe. Este un solvent excelent; dizolvă multe alte substanțe și permite acestor substanțe să reacționeze atunci când sunt în soluție., De fapt, apa este uneori numită solvent universal datorită acestei abilități. Apa are puncte de topire și fierbere neobișnuit de mari (0°C și respectiv 100°C) pentru o moleculă atât de mică. Punctele de fierbere pentru molecule de dimensiuni similare, cum ar fi metanul (BP = -162°C) și amoniacul (BP = -33°C), sunt cu mai mult de 100° mai mici. Deși un lichid la temperaturi normale, moleculele de apă experimentează o interacțiune intermoleculară relativ puternică, care le permite să mențină faza lichidă la temperaturi mai ridicate decât se aștepta.,spre deosebire de majoritatea substanțelor, forma solidă a apei este mai puțin densă decât forma sa lichidă, ceea ce permite gheții să plutească pe apă. Configurația cea mai favorabilă din punct de vedere energetic a moleculelor H2O este una în care fiecare moleculă este legată de hidrogen la patru molecule vecine. Datorită mișcărilor termice, acest ideal nu este niciodată atins în lichid, dar când apa îngheață la gheață, moleculele se așează exact în acest tip de aranjament în cristalul de gheață., Acest aranjament necesită ca moleculele să fie oarecum mai îndepărtate decât ar fi altfel; ca o consecință, gheața, în care legătura de hidrogen este la maxim, are o structură mai deschisă și, astfel, o densitate mai mică decât apa.,
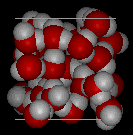
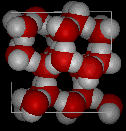
Iată vederi tridimensionale ale unei structuri locale tipice de apă (stânga) și gheață (dreapta.) Observați o deschidere mai mare a structurii de gheață care este necesară pentru a asigura cel mai puternic grad de lipire a hidrogenului într-o rețea cristalină uniformă și extinsă. Structura apei lichide este foarte asemănătoare, dar în lichid, legăturile de hidrogen sunt rupte continuu și formate din cauza mișcării moleculare rapide. Deoarece gheața este mai puțin densă decât apa lichidă, râurile, lacurile și oceanele îngheață de sus în jos., De fapt, gheața formează un strat protector de suprafață care izolează restul apei, permițând peștilor și altor organisme să supraviețuiască în nivelurile inferioare ale unui lac sau mare înghețat. Dacă gheața ar fi mai densă decât lichidul, gheața formată la suprafață pe vreme rece s-ar scufunda la fel de repede pe cât s-ar forma. Corpurile de apă ar îngheța de jos în sus, ceea ce ar fi letal pentru majoritatea creaturilor acvatice. Extinderea apei la îngheț explică, de asemenea, de ce motoarele auto sau cu barca trebuie protejate de „antigel” și de ce conductele neprotejate din case se sparg dacă li se permite să înghețe.,apa necesită, de asemenea, o cantitate neobișnuit de mare de energie pentru a schimba temperatura. În timp ce 100 J de energie va schimba temperatura de 1 g de Fe Cu 230°C, aceeași cantitate de energie va schimba temperatura de 1 g de H2O cu doar 100°C. Astfel, apa își schimbă temperatura încet pe măsură ce căldura este adăugată sau îndepărtată. Acest lucru are un impact major asupra vremii, deoarece sistemele de furtună precum uraganele pot fi afectate de cantitatea de căldură pe care apa oceanului o poate stoca.influența apei asupra lumii din jurul nostru este afectată de aceste proprietăți., Nu este fascinant că o moleculă atât de mică poate avea un impact atât de mare?