până acum, toate reacțiile noastre au avut loc în condiții ideale. Cu toate acestea, condițiile ideale nu există în viața reală. Reactanții pot fi impuri, reacțiile nu pot merge la finalizare sau reacțiile date pot trebui să concureze cu mai multe reacții adverse mai mici. De fapt, în laborator, dacă primiți 60% din cantitatea așteptată de produs, care este considerat foarte bun.
acum, să vorbim terminologie. Cantitatea calculată sau așteptată a produsului se numește randamentul teoretic., Cantitatea de produs efectiv produsă se numește randamentul real. Când împărțiți randamentul real cu randamentul teoretic, obțineți un procent zecimal cunoscut sub numele de randamentul procentual al unei reacții.
la Sută Randament = 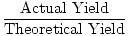 |
din nou, e timpul pentru un exemplu de problemă:
Problema: care este procentul de randament dintre următoarele reacții 60 de grame de CaCO3 este încălzit pentru a da 15 grame de CaO?,
| CaCO3→CaO + CO2 |
Soluție: în mod Ideal, cât de multe grame de CaO ar trebui să fie produse? Mai întâi verificați ecuația este echilibrată; este. Acum convertiți-vă la alunițe, pe baza cantității de CaCO3 prezente.
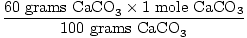 × ×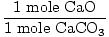 = 0.6 mol CaO = 0.6 mol CaO |
Cât de multe de grame este asta?,
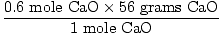 = 33.6 g CaO = 33.6 g CaO |
Deci, în mod ideal, 33.6 de grame de CaO ar fi fost produs în această reacție. Acesta este randamentul teoretic. Cu toate acestea, problema ne spune că au fost produse doar 15 grame. 15 grame este randamentul real. Acum este o chestiune simplă de a găsi randament la sută.