 General
General
Hafniu este un element chimic cu simbolul Hf și numărul atomic 72. Acesta este numit după numele Latin al orașului Copenhaga, Hafniain care elementul a fost descoperit. Este un metal de tranziție gri-argintiu, strălucitor, rezistent la coroziune, care se află în al 4-lea subgrup (Grupa 4) sau grup de titan din tabelul periodic.,
hafniul are proprietăți foarte asemănătoare cu zirconiul direct deasupra acestuia în tabelul periodic. Funcțiile biologice nu sunt cunoscute, nu apar în mod normal în organismul uman și nu sunt toxice.
hafniul a fost unul dintre ultimele elemente stabile din tabelul periodic care a fost descoperit. Prima indicație a existenței unui alt element între lutețiu și tantal a apărut din Legea lui Moseley Găsită în 1912., În 1914, Henry Moseley a încercat să găsească elementul necunoscut, dar așteptat, cu numărul atomic 72 conform acestei legi în eșantioane de minerale de pământuri rare (în prezent lantanide). Dar nu a reușit.
în lucrarea sa despre teoria atomică publicată în 1922, Niels Bohr a prezis că seria de lantanide cu lutețiu se va încheia și că elementul 72 trebuie, prin urmare, să fie similar cu zirconiul. Hafniul ar putea fi detectat doar un an mai târziu: în 1923, Dirk Coster și George de Hevesy l-au descoperit la Copenhaga folosind spectroscopia cu raze X în zirconiul norvegian., Investigarea ulterioară a altor minerale a arătat că hafniul este întotdeauna conținut în minerale care conțin zirconiu. Jantzen și Hevesy au reușit să le separe de zirconiu prin cristalizarea repetată a diamoniu și a fluorurilor dipotasice ale celor două elemente. Hafniul elementar ar putea fi apoi obținut prin reducerea cu sodiu.
eveniment
Hafniu, cu un conținut de 4,9 ppm în crusta continentală, este un element care nu este foarte comun de pe pământ., În ceea ce privește frecvența, este comparabil cu elementele brom și cesiu și mai frecvent decât aurul și mercurul cunoscut de mult timp. Hafniul nu apare în mod natural sau în propriile minerale. Mineralele de zirconiu, cum ar fi zirconul și baddeleyitul, pe de altă parte, conțin întotdeauna hafniu; cantitatea de hafniu este de obicei 2% din conținutul de zirconiu (1-5% în greutate de hafniu). Unul dintre puținele minerale care conțin mai mult hafniu decât zirconiu este soiul zircon alvit .,
analog cu zirconiul, cele mai importante depozite de hafniu sunt depozitele de zirconiu din Australia și Africa de Sud. Rezervele sunt estimate la 1,1 milioane de tone (calculate ca oxid de hafniu).
Extracție și de prezentare
În scopul de a obține hafniu, trebuie să fie separate de zirconiu. Acest lucru nu este posibil în timpul procesului de fabricație, dar are loc într-un proces separat. Procesele de extracție sunt utilizate pentru separare., Se utilizează solubilitatea diferită a anumitor săruri de zirconiu și hafniu în solvenți speciali. Exemple în acest sens sunt solubilitățile diferite ale nitraților din fosfatul de tri-n-butil și cea a tiocianaților din metil izobutil cetonă. Alte opțiuni posibile de separare sunt schimbătoarele de ioni și distilarea fracționată a compușilor adecvați.
după procesul Kroll, hafniul separat poate fi mai întâi transformat în clorură de hafniu (IV) și apoi redus la hafniu elementar cu sodiu sau magneziu.,
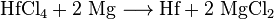
Dacă chiar mai pură hafniu este necesar, Van Arkel de Boer proces poate fi folosit. În timpul încălzirii sub vid, hafniul reacționează inițial cu iodul pentru a forma iodură de hafniu (IV). Acesta este împărțit din nou în hafniu și iod pe un fir fierbinte.

Hafniu este produs numai în cantități mici pe o scară de 100 de tone., Nu este produs intern, ci este un produs secundar al extracției de zirconiu fără hafniu pentru tije de combustibil.
Proprietati
Proprietăți Fizice

structura cristalelor de α-Hf, o = 320 pm,c = 505 pm
Hafniu este un argintiu, strălucitor heavy metal de înaltă densitate (13,31 g / cm3). Se cristalizează în două modificări diferite în funcție de temperatură., În condiții normale, cristalizează într-un ambalaj hexagonal apropiat de sfere (α-Hf) și, prin urmare, este izotipic la α-Zr, peste 1775 ° C se transformă într-o structură cubică centrată pe corp (β-Hf).
dacă puritatea hafniului este ridicată, este relativ moale și pliabilă. Este ușor de lucrat prin rulare, forjare și ciocănire. Dacă, pe de altă parte, există urme de oxigen, azot sau carbon în material, acesta devine fragil și dificil de procesat., Punctele de topire și fierbere ale hafniului sunt cele mai ridicate din grup la 2227 ° C și 4450 ° c (punct de topire: Titan: 1667 ° c, zirconiu: 1857 ° c).
În aproape toate celelalte proprietăți, metal seamănă cu bricheta omolog de zirconiu. Aceasta este cauzată de contracția lantanidei, care provoacă raze Atomice și ionice similare (raze atomice Zr: 159 pm, Hf: 156 pm). O excepție este densitatea zirconiului cu 6,5 g / cm3 are o valoare semnificativ mai mică. O diferență importantă din punct de vedere tehnic este că hafniul poate absorbi neutronii de 600 de ori mai bine., Acesta este motivul pentru care hafniul trebuie separat pentru utilizarea zirconiului în centralele nucleare.
Hafniu este supraconductoare sub temperatura de tranziție de 0,08 K.
proprietăți Chimice
Hafniu este un metal de bază, care reacționează cu oxigenul pentru a forma dioxid de hafniu atunci când este încălzit. Alte nemetale, cum ar fi azotul, carbonul, borul și siliciul, formează, de asemenea, compuși în aceste condiții., Un strat dens de oxid se formează rapid la temperatura camerei, care pasivizează metalul și îl protejează de oxidarea ulterioară.
hafniul este stabil în majoritatea acizilor datorită pasivării sale în condiții normale. Se corodează rapid în acidul fluorhidric; coroziunea vizibilă apare în acidul sulfuric și fosforic fierbinte, concentrat. Amestecurile de acid clorhidric-acid azotic, inclusiv aqua regia, trebuie expuse la hafniu doar pentru o perioadă scurtă de timp, chiar și la temperatura camerei; la 35 ° C, trebuie așteptate rate de eliminare mai mari de 3 mm / an., În baze apoase este rezistent până la o temperatură de aprox. 100 ° C, îndepărtarea materialului este de obicei mai mică de 0,1 mm / an.
izotop
Există un total de 35 de izotopi și 18 nucleare izomeri de hafniu 153Hf să 188Hf cunoscut. Hafniul Natural este un element mixt care constă dintr-un total de șase izotopi diferiți. Cel mai frecvent izotop este cu o frecvență de 35,08% 180hf. Rezultă 178Hf cu 27,28%, 177Hf cu 18,61%, 179Hf cu 13,62%, 176Hf cu 5,27% și 174Hf la 0,16%., Singurul izotop natural este 174hf slab radioactiv, este un emițător alfa cu un timp de înjumătățire de 2 x 1015 ani. Izotopii 177hf și 179hf pot fi detectați cu ajutorul spectroscopiei RMN.
nucleul izomer 178 2mWith un timp de înjumătățire de 31 de ani, Hf este de lungă durată și, în același timp, emite puternice radiații gamma de 2,45 MeV, atunci când acesta se descompune. Aceasta este cea mai mare energie pe care o emite un izotop care este stabil pe o perioadă lungă de timp. O posibilă aplicație este utilizarea acestui izomer de bază ca sursă în lasere puternice., În 1999, Carl Collins a descoperit că izomerul își poate elibera energia într-o singură lovitură atunci când este expus la raze X. Cu toate acestea, posibilele aplicații, cum ar fi explozivii, sunt puțin probabile.
Utilizare
Hafniu foaie de deșeuri industriale
Pentru că este dificil de extras, hafniu este folosit doar în cantități mici. Domeniul principal de aplicare este tehnologia nucleară, în care hafniul este utilizat ca tijă de control pentru reglarea reacției în lanț în reactoarele nucleare., Utilizarea hafniului are mai multe avantaje față de alte substanțe posibile de absorbție a neutronilor. Elementul este foarte rezistent la coroziune, iar reacția nucleară cu neutronii creează izotopi de hafniu, care au și secțiuni transversale de absorbție ridicate. Datorită prețului ridicat, este adesea potrivit doar pentru aplicații militare, de exemplu pentru reactoarele din submarinele atomice.
există câteva alte utilizări., Hafniul reacționează rapid cu cantități mici de oxigen și azot și, prin urmare, poate fi utilizat ca substanță getter pentru a elimina cele mai mici cantități din aceste substanțe din sistemele de vid ultra-înalte. Când este ars, metalul emite o lumină foarte puternică. Prin urmare, este posibil să se utilizeze hafniu în lămpi flash cu o eficiență luminoasă deosebit de ridicată. Mai mulți compuși foarte stabili și cu topire ridicată, în special nitrura de hafniu și carbura de hafniu, pot fi făcuți din elemente.,
în aliaje cu metale precum niobiu, tantal, molibden și tungsten, o adăugare de 2% hafniu crește rezistența. Sunt create materiale deosebit de stabile, cu topire ridicată și rezistente la căldură.
instrucțiuni de siguranță
la fel Ca multe alte metale, hafniu este foarte inflamabil și piroforice în fin divizate de stat. În schimb, nu este inflamabil atunci când este compact. Metalul nu este toxic. Din aceste motive, nu trebuie respectate reglementări speciale de siguranță la manipularea hafniului.,
Conexiuni
Hafniu formează un număr de compuși. Acestea sunt în mare parte săruri sau cristale mixte și au adesea puncte de topire ridicate. Cea mai importantă stare de oxidare a hafniului este + IV, dar compușii în stări de oxidare mai mici, de la 0 la + III, iar în complexe sunt cunoscute și stări de oxidare negative.
Hafniu (IV) oxid
Hafniu (IV) oxid este foarte stabil și de înaltă de topire solid. Are o permitivitate relativă ridicată de 25 (pentru comparație: dioxid de siliciu: 3,9)., Prin urmare, poate fi folosit ca un dielectric high-k pentru a izola conexiunea de control (poarta) pentru microprocesoare. Prin reducerea în continuare a lățimilor structurii, curenții de scurgere devin o problemă din ce în ce mai mare, deoarece miniaturizarea structurilor CMOS necesită, de asemenea, o izolare mai subțire a porții. Curentul de scurgere nedorit crește brusc sub 2 nm datorită efectului tunelului. Prin utilizarea unui dielectric de înaltă k, grosimea dielectricului poate fi crescută din nou pentru a reduce curentul de scurgere fără ca tranzistorul să aibă o pierdere de performanță (reducerea vitezei de comutare)., Astfel, dielectricii mai groși permit miniaturizarea ulterioară.
Alte hafniu compuși
Hafniu carbură este una dintre substanțele cu cele mai ridicate puncte de topire. Împreună cu nitrura de hafniu și borura de hafniu, aparține materialelor dure.
există unii compuși halogeni cunoscuți de hafniu. În starea de oxidare + IV există atât fluorura, cât și clorura, bromura și iodura. Clorura de hafniu (IV) și iodura de hafniu (IV) joacă un rol în producerea hafniului., În stările de oxidare inferioară sunt cunoscuți numai compușii de clor și brom și iodura de hafniu (III).
potasiu hexafluoridohafnate (IV) K2 precum și amoniu hexafluoridohafnate (IV) (NH4)2 poate fi folosit pentru a separa hafniu din zirconiu, atât sărurile sunt mai solubile decât cele corespunzătoare zirconiu complexe.,
→ Hf + 2 H2O)
| isotope | NH | t1/2 | ZA | ZE (MeV) | ZP |
|---|---|---|---|---|---|
| 174Hf | 0,162% | 2 · 1015 a | α | 2,495 | 170Yb |
| 175Hf | {Syn.,r
Light- (F)
|
||||
| R and S phrases | R: 17 | ||||
| S: no phrases |
